「新薬の3分の1が、承認後に安全性の問題発覚」のFDA、ファイザーのコロナワクチン正式承認
世界中で新型コロナウイルスワクチンの接種が進められている中にあって、“コロナ前”の2017年に発表された研究論文が再び脚光を浴びている。FDAに承認された新薬の3分の1がその後になって安全性の問題を抱えているというのである。
■FDAが承認した新薬の3分の1に安全性の懸念
米ファイザー社製などの新型コロナウイルスワクチンはご存知のようにすでに世界中で大勢の人々が接種している現実の中、意外にもつい先日の8月23日に米食品医薬品局(FDA)がファイザー社製ワクチンを“正式承認”した。
いずれにしても新型コロナウイルスのワクチンに関しては特例的な措置で各国の保健当局が暫定的に承認、認可をしているわけだが、こうした状況の中にあってコロナの“コ”の字もなかった2017年の研究論文が再び注目されているのだ。2001年から2010年までにFDAによって承認された新薬の3分の1が市場に出回った後になってから重大な安全上の問題を抱えていることが浮き彫りにされたのである。
米・イェール大学をはじめとする合同研究チームが2017年5月に「Journal of the American Medical Association 」で発表した研究では、2001年から2010年の10年間にFDAに承認された222の新薬のうち、71が承認を取り下げられ、副作用に関する警告が必要であるか、新しいリスクについての安全性の発表が必要であったことが報告されている。
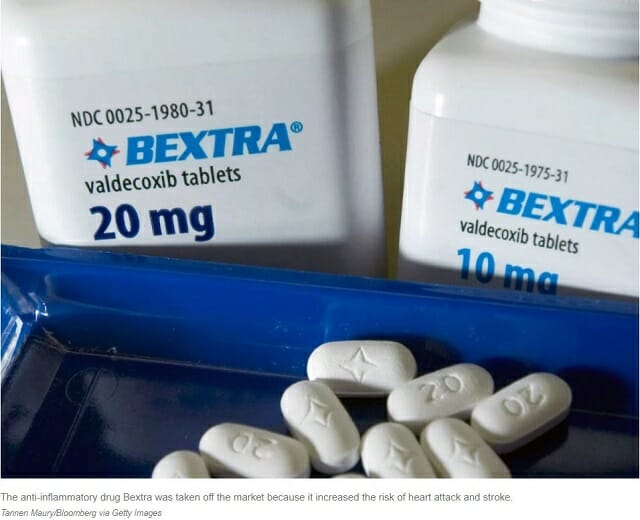
「政権は規制の緩和と承認の迅速化を推進していますが、これらの決定は結果をもたらします」と研究チ―ムのジョセフ・ロス博士は語る。
イェール大学の研究者の以前の研究では、FDAはヨーロッパの対応機関よりも早く薬を承認し、薬の承認における重要な試験の大部分は1000人未満の患者を対象とし、期間も6カ月以内であったと結論づけられている。
研究によると、安全性の懸念が明らかになるまでの期間は、薬が承認されてから中央値で4.2年。また、「精神科の薬」「生物学的薬」「承認までの期間が短い薬」「承認の規制期限近くになって承認された薬」でより問題が起きやすかった。
承認までの期間を短縮することが求められている中にあって、承認から市販後になって安全性が疑われるケースが増えているということは、患者に実際に使ってみることで安全性のデータが収集されるという、ある意味で“人体実験”の様相すら呈していることになる。
関連記事
人気連載
“包帯だらけで笑いながら走り回るピエロ”を目撃した結果…【うえまつそうの連載:島流し奇譚】
現役の体育教師にしてありがながら、ベーシスト、そして怪談師の一面もあわせもつ、う...
2024.10.02 20:00心霊「新薬の3分の1が、承認後に安全性の問題発覚」のFDA、ファイザーのコロナワクチン正式承認のページです。医療、新薬、ワクチン、FDA、製薬、臨床試験、治験、ビッグファーマなどの最新ニュースは好奇心を刺激するオカルトニュースメディア、TOCANAで